
El tratamiento de HPN de Apellis Pharmaceuticals recibe la designación Fast Track
Este medicamento está diseñado para pacientes que experimentan hemólisis y requieren transfusiones de glóbulos rojos incluso mientras toman Eculizumab.
Apellis Pharmaceuticals (EEUU) ha anunciado que su medicamento huérfano APL-2, para el tratamiento de la Hemoglobinuria Nocturna Paroxística (HPN), recibió la designación Fast Track (procedimiento de aprobación por vía rápida) por la FDA (Food and Drug Administration – Agencia de Alimentos y Medicamentos del gobierno de EE UU).
Este medicamento está diseñado para pacientes que experimentan hemólisis y requieren transfusiones de glóbulos rojos incluso mientras toman Eculizumab.
APL-2 se ejecuta actualmente en dos ensayos clínicos en fase Ib. Un ensayo clínico evaluó las dosis de APL-2 administradas por inyección subcutánea diaria (SC) en pacientes con HPN que no recibieron anteriormente el estándar de atención; y el otro ensayo, evaluó las dosis de APL-2 como complemento en la atención estándar.
Resultados
Las dosis de APL-2 de 180 mg y 270 mg redujeron significativamente la actividad hemolítica en tan sólo ocho días después de iniciar del tratamiento; y esta inhibición se mantuvo además durante todo el período de dosificación.
Acerca de APL-2
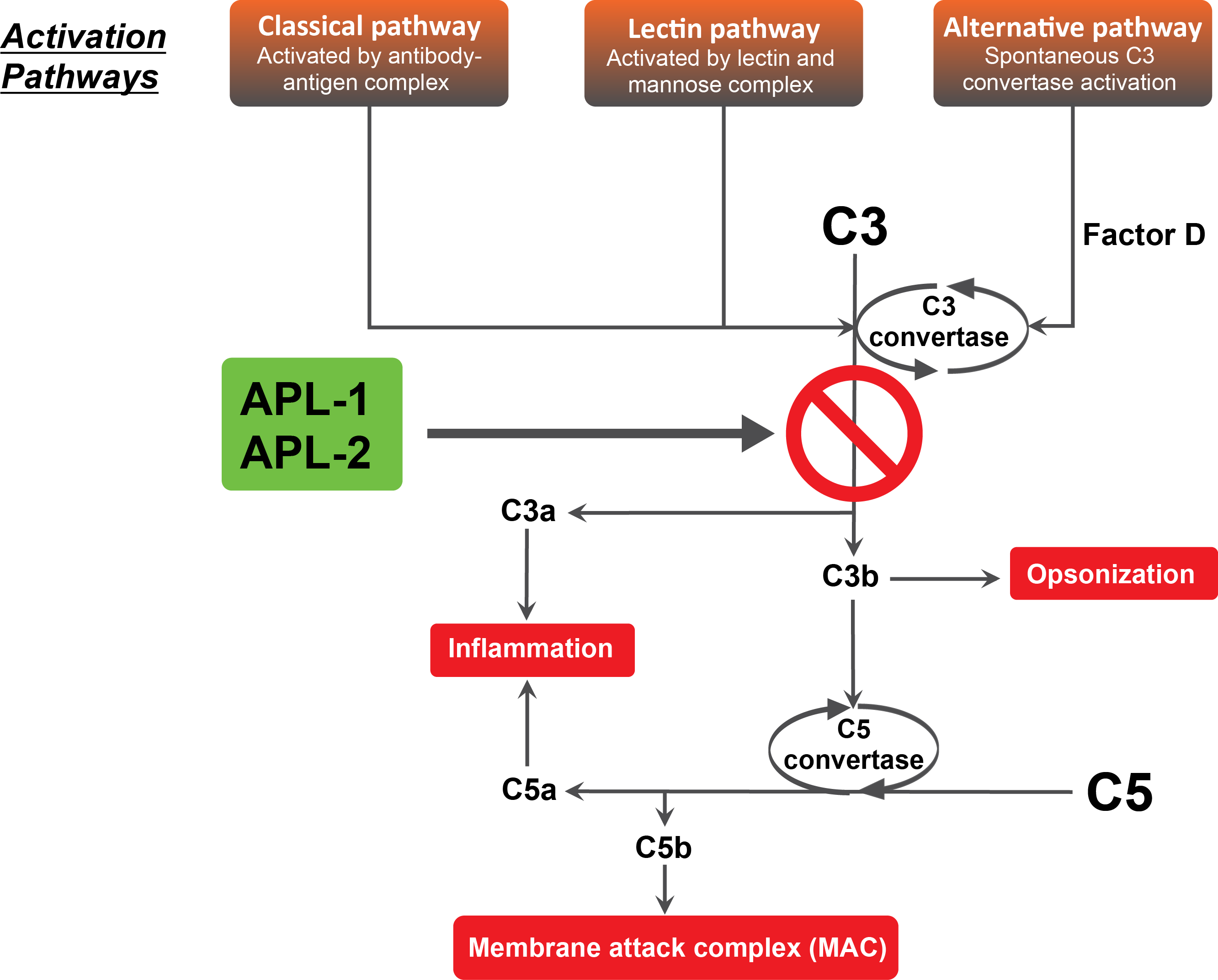
El APL-2 actúa en C3 y C3b, bloqueando de forma efectiva las tres vías de activación del complemento (clásica, lectina y alternativa) con una potencia particularmente alta respecto la vía alternativa.
Acerca de la designación `Fast Track´
El programa Fast Track de la FDA está diseñado para facilitar y acelerar el desarrollo y revisión de nuevos fármacos.
FUENTE: http://www.raredr.com/news/paroxysmal-nocturnal-hemoglobinuria-fast-track-designation



























